Anomalie d’Ebstein
Introduction
Définition
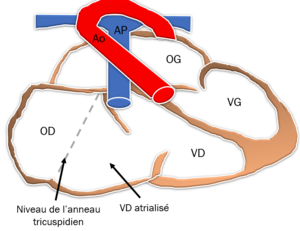
La maladie d’Ebstein se définit par un déplacement apical de la valve tricuspide, un défaut de délamination des feuillets septal et postérieur associé à un feuillet antérieur allongé et présentant une déformation « en voile ». Il en résulte un ventricule droit divisé en une portion « atrialisée » et une portion fonctionnelle de petit volume.
Epidémiologie
Concerne environ 1/200.000 naissances vivantes, soit un peu moins de 1% des cardiopathies congénitales. Le diagnostic peut être fait en anténatal lors des échographies trimestrielles. En fonction de la sévérité de la maladie, le diagnostic peut s’étendre de la période néonatale (nouveau-né cyanosé avec foie cardiaque) jusqu’à la vie adulte (simple limitation à l’effort).
Physiopathologie
La sévérité de la maladie va être conditionnée par l’accolement des feuillets septal et postérieur de la valve tricuspide le long de la paroi ventriculaire droite. Plus cet accolement est important, plus le ventricule droit résiduel sera réduit, et la maladie de révélation précoce. En effet, la gêne au remplissage d’un ventricule droit de petite dimension, associée à une fuite tricuspidienne, va occasionner une élévation importante des pressions atriales droites et des structures en amont. Le nouveau-né présente donc une hépatomégalie associée à une cyanose intense par shunt droite-gauche au travers du foramen ovale. La chute des pressions pulmonaires lors des premiers jours de vie, va entrainer une diminution voire une disparition complète de la cyanose.
Différentes anomalies peuvent être associées à une maladie d’Ebstein :
- Des faisceaux accessoires retrouvés chez 25% des patients et multiples dans 1/3 des cas.
- Une CIA secundum ou un FOP.
- Et des malformations diverses : Non compaction VG, maladie mitrale, sténose pulmonaire, obstruction de la chambre de chasse VD, hypoplasie de l’artère pulmonaire.
Diagnostic
Clinique
Comme vu précédemment, le spectre clinique est large et hétérogène, allant de formes mineures asymptomatiques, à des formes sévères de révélation néonatales.
On peut ainsi retrouver une cyanose avec hépatomégalie néonatale. Dans les formes moins sévères, la révélation l’âge adulte peut être le fait de l’exploration d’une dyspnée, de palpitations, de signes congestifs droits.
L’auscultation cardiaque objective un dédoublement du B1 avec augmentation de l’intensité de T1. Le B2 peut également être dédoublé, associé à un B3 droit. L’insuffisance tricuspide va donner lieu à un souffle systolique maximal à la xyphoïde.
Electrocardiogramme
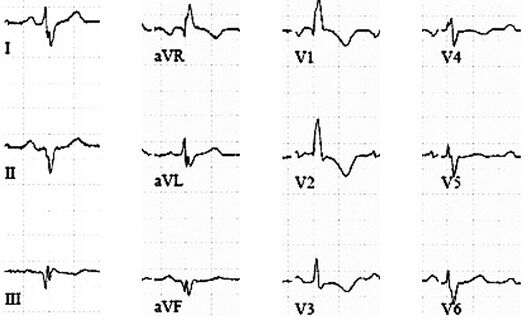
Ondes P « Himalayennes », bloc de branche droit, ondes Q de V1 à V4 et en inférieur, FA-flutter.
La prévalence d’une voie accessoire est estimée entre 6 et 30% des patients atteints de maladie d’Ebstein. La localisation préférentielle de la voie accessoire est postéro-septale droite.
Radiographie thoracique
De face, le cœur présente un aspect de « bouteille d’eau » du fait d’une convexité gauche secondaire à une dilatation de l’infundibulum ventriculaire droit.
Echocardiographie
L’échocardiographie demeure l’examen clé dans le diagnostic et la recherche des comorbidités associées à la maladie d’Ebstein. L’existence d’un décalage mitro-tricuspidien > 8 mm/m² de surface corporelle signe la maladie d’Ebstein.
Evolution
Survie
La mortalité opératoire auparavant élevée (>25%) est tombée à <6% dans les centres spécialisés. Plus de 90% des patients opérés par un chirurgien expérimenté survivent >10 ans, beaucoup en classe fonctionnelle I ou II. Les décès tardifs sont probablement dus à des arythmies. Dans une grande série, la survie sans réopération tardive était de 86 %, 74 %, 62 % et 46 % à 5, 10, 15 et 20 ans, respectivement.
Complications
Les complications potentielles de cette cardiopathie congénitale sont :
- L’insuffisance tricuspidienne sévère
- L’insuffisance cardiaque droite secondaire à la dilatation cavitaire droite
- La survenue d’arythmies supraventriculaires à type de flutter auriculaire, fibrillation atriale ou tachycardie réentrante orthodromique ou antidromique en fonction de la présence de voies accessoires.
- En cas d’association à une CIA, la survenue d’embolies paradoxales ou de cyanose.
- Une obstruction de la chambre de chasse ventriculaire droite par la valve tricuspide anormale.
La grossesse est contre-indiquée en cas de SaO2 < 85% et/ou de signes d’insuffisance cardiaque.
Traitement
En période néonatale, le traitement repose sur les vasodilateurs pulmonaires (NO), la ventilation artificielle et le traitement diurétique.
Les indications à la réalisation d’une intervention sont :
- La persistance, au-delà d’un mois.
- L’insuffisance tricuspidienne avec insuffisance cardiaque symptomatique ou détérioration de la capacité fonctionnelle ou dysfonction ventriculaire droite progressive (classe I)
- L’insuffisance tricuspidienne significative avec dilatation ventriculaire droite progressive, la persistance d’une cyanose au-delà d’un mois (shunt droit → gauche) ou la survenue d’embolies paradoxales (classe II). Toute fermeture de CIA devra être soigneusement argumentée car susceptible d’aggraver l’hyperpression droite.
- L’ablation par cathéter de faisceaux accessoires à haut risque ou multiples (classe I). Il faut noter que la chirurgie réparatrice peut fortement entraver la faisabilité d’une ablation de voie accessoire. Il est donc largement admis d’effectuer une exploration électrophysiologiques endocavitaire avant toute réparation chirurgicale.
Les modalités opératoires vont comprendre :
- La réparation valvulaire dont la faisabilité va dépendre de la longueur et de la mobilité du feuillet antérieur de la valve tricuspide afin de permettre la création d’une valve à mono-feuillet, ainsi que de la taille du ventricule droit fonctionnel (> 1/3 du ventricule droit total).
- La réalisation d’une procédure de Glenn (anastomose cavo-pulmonaire supérieure bidirectionnelle) doit s’envisager en présence d’une dilatation ou dysfonction ventriculaire droite sévère. Elle est à éviter en cas dysfonction ventriculaire gauche ou d’élévation des pressions télédiastoliques de l’oreillette gauche.
- La réalisation d’un remplacement valvulaire tricuspide conventionnel.
- La réalisation d’une plicature sélective du ventricule droit atrialisé.
- La réalisation d’une procédure de Fontan en cas de ventricule droit hypoplasique, consistant en l’exclusion des cavités droites par la ligature du tronc pulmonaire et l’anastomose des VCS et VCI (par l’intermédiaire d’un conduit extra-cardiaque) aux branches artérielles pulmonaires.
- Le recours à la greffe cardiaque en cas d’échec de réparation ou de dysfonction biventriculaire sévère.