« BAV congénital » : différence entre les versions
| Ligne 10 : | Ligne 10 : | ||
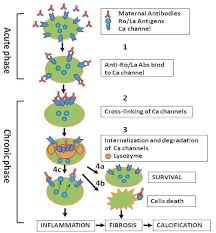
Il s'agit dans 95% des cas d'un BAV immunologique secondaire à la présence d'anticorps anti SSA /anti SSB chez la mère.En effet, ces anticorps entraîne un processus d'inflammation locale puis de fibrose des tissus conductifs cardiaques, avec des troubles conductifs par la suite irréversibles .Environ 2 à 5% des nouveaux-nés de mères présentant des anticorps antiSSA/SSB vont développer un BAV, avec un risque de récidive lors d'une prochaine grossesse de 12 à 25% en cas d'antécédent de BAV immun.La mortalité en période foetale et néonatale est de 15% , la présence d'un anasarque foetal et/ou d'un échappement ventriculaire inférieur à 55 bpm étant associée à un sur-risque de mortalité. | Il s'agit dans 95% des cas d'un BAV immunologique secondaire à la présence d'anticorps anti SSA /anti SSB chez la mère.En effet, ces anticorps entraîne un processus d'inflammation locale puis de fibrose des tissus conductifs cardiaques, avec des troubles conductifs par la suite irréversibles .Environ 2 à 5% des nouveaux-nés de mères présentant des anticorps antiSSA/SSB vont développer un BAV, avec un risque de récidive lors d'une prochaine grossesse de 12 à 25% en cas d'antécédent de BAV immun.La mortalité en période foetale et néonatale est de 15% , la présence d'un anasarque foetal et/ou d'un échappement ventriculaire inférieur à 55 bpm étant associée à un sur-risque de mortalité. | ||
[[Fichier:Image.png| | [[Fichier:Image.png|droite|sans_cadre]] | ||
La deuxième étologie en terme de prévalence est associée à une cardiopathie congénitale , notamment les transpositons des gros vaisseaux, les canaux atro-ventriculaires, les hétérotaxies et les doubles discordances. | La deuxième étologie en terme de prévalence est associée à une cardiopathie congénitale , notamment les transpositons des gros vaisseaux, les canaux atro-ventriculaires, les hétérotaxies et les doubles discordances. | ||
Version du 3 avril 2023 à 14:46
Le BAV congénital est un trouble conductif atrio-ventriculaire diagnostiqué en période foetale , à la naissance ou dans le premier mois de vie.
Epidémiologie et étiologies
La prévalence d'un BAV congénital sans cardiopathie associée est estimée actuellement à 1/15 000 à 1/20 000 naissances par an.
La prévalence d'un BAV congénital sans cardiopathie associée est estimée actuellement à 1/15 000 à 1/20 000 naissances par an.
Il s'agit dans 95% des cas d'un BAV immunologique secondaire à la présence d'anticorps anti SSA /anti SSB chez la mère.En effet, ces anticorps entraîne un processus d'inflammation locale puis de fibrose des tissus conductifs cardiaques, avec des troubles conductifs par la suite irréversibles .Environ 2 à 5% des nouveaux-nés de mères présentant des anticorps antiSSA/SSB vont développer un BAV, avec un risque de récidive lors d'une prochaine grossesse de 12 à 25% en cas d'antécédent de BAV immun.La mortalité en période foetale et néonatale est de 15% , la présence d'un anasarque foetal et/ou d'un échappement ventriculaire inférieur à 55 bpm étant associée à un sur-risque de mortalité.
La deuxième étologie en terme de prévalence est associée à une cardiopathie congénitale , notamment les transpositons des gros vaisseaux, les canaux atro-ventriculaires, les hétérotaxies et les doubles discordances.
Le BAV congénital idiopathique est une pathologie très rare avec une prévalence de moins de 1 cas pour 200 000 naissances.Il doit faire rechercher une cause génétique telle la PCCD ( Progressive cardiac conduction disease ) dans laquelle des mutations peuvent être retrouvées ( gènes SCN5A, SCN1B, SCN10A, TRPM4, et KCNK1 notamment ).
Les mutations du gène SCN5A peuvent également traduire un syndrome du QT long, notamment de type 2 ou de type 3 , pouvant se révéler en période néonatale par des troubles conductifs atrio-ventriculaires ; ces formes sont d'ailleurs associées à un plus mauvais pronostic.
Enfin, des étiologies plus rares en période néonatale peuvent être recherchées, comme une myocardite ( maladie de Lyme notamment) , une pathologie métabolique ou neuromusculaire.
Présentation clinique
En période foetale, le tableau clinique repose sur une fréquence ventriculaire inférieure à 100 bpm parfois associée à un anasarque.Il s'agit dans 80% des cas d'un BAV complet.En cas d'étiologie immune, une atteinte myocardique et endocardique peut être retrouvée : anomalie valvulaire, cardiomyopathie dilatée, fibroélastose.
Les formes découvertes plus tardivement, plusieurs semaines après la naissance, sont génaralement de melleur pronostic.
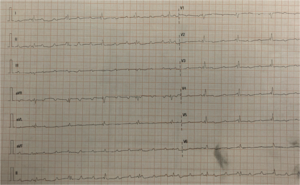
ECG d'un BAV congénital immun chez un nouveau-né :
Indications de stimulation
Les indications de stimulation cardiaque face à un BAV congénital sont : la présence de symptômes ; la présence d'un retentissement du trouble conductif sur la fonction ventriculaire avec notamment dilatation du ventricule gauche ; certains critères tels une fréquence cardiaque moyenne inférieure à 55 bpm chez le nouveau-né et nourrisson ( inférieure à 50 bpm après 2 ans ) ou 70 bpm en cas de cardiopathie associée ; la présence d'arythmie ventriculaires ; la présence d'allongement du QT ; des pauses supérieures à 3 fois le RR.
| Indications de stimulation | |
|---|---|
| Symptômes |
|
| Echographiques |
|
| Prophylactiques |
|
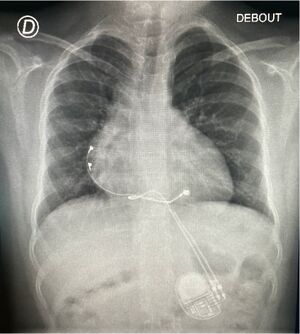
L'implantation d'un matériel par voie épicardique est privilégiée chez l'enfant , en particulier pour un poids inférieur à 20 kg , avec une sonde ventriculaire fixée au niveau du ventricule gauche afin de diminuer le risque de cardiopathie induite par la stimulation permanente. Chez le nouveau-né et le nourrisson , une seule sonde ventriculaire est généralement implantée avec une stimulation programmée en VVIR.
- ↑ Balmer C, Fasnacht M, Rahn M, Molinari L, Bauersfeld U. Long-term follow up of children with congenital complete atrioventricular block and the impact of pacemaker therapy. Europace. oct 2002;4(4):345‑9.
- ↑ Baruteau AE, Pass RH, Thambo JB, Behaghel A, Le Pennec S, Perdreau E, et al. Congenital and childhood atrioventricular blocks: pathophysiology and contemporary management. Eur J Pediatr. sept 2016;175(9):1235‑48.
- ↑ Breur JMPJ, Kapusta L, Stoutenbeek P, Visser GHA, van den Berg P, Meijboom EJ. Isolated congenital atrioventricular block diagnosed in utero: natural history and outcome. J Matern Fetal Neonatal Med. juill 2008;21(7):469‑76.
- ↑ Hunter LE, Simpson JM. Atrioventricular block during fetal life. J Saudi Heart Assoc. 2015 Jul;27(3):164-78. doi: 10.1016/j.jsha.2014.07.001. Epub 2014 Jul 10. PMID: 26136631; PMCID: PMC4481419.
- ↑ Gozar L, Marginean C, Fagarasan A, Muntean I, Cerghit-Paler A, Miklosi D, Toganel R. Congenital complete atrioventricular block from literature to clinical approach - a case series and literature review. Med Ultrason. 2021 May 20;23(2):188-193. doi: 10.11152/mu-2723. Epub 2020 Dec 5. PMID: 33626113.
- ↑ Writing Committee Members; Shah MJ, Silka MJ, Silva JNA, Balaji S, Beach CM, Benjamin MN, Berul CI, Cannon B, Cecchin F, Cohen MI, Dalal AS, Dechert BE, Foster A, Gebauer R, Gonzalez Corcia MC, Kannankeril PJ, Karpawich PP, Kim JJ, Krishna MR, Kubuš P, LaPage MJ, Mah DY, Malloy-Walton L, Miyazaki A, Motonaga KS, Niu MC, Olen M, Paul T, Rosenthal E, Saarel EV, Silvetti MS, Stephenson EA, Tan RB, Triedman J, Bergen NHV, Wackel PL. 2021 PACES Expert Consensus Statement on the Indications and Management of Cardiovascular Implantable Electronic Devices in Pediatric Patients. Heart Rhythm. 2021 Nov;18(11):1888-1924. doi: 10.1016/j.hrthm.2021.07.038. Epub 2021 Jul 29. PMID: 34363988.
- ↑ Lupoglazoff JM, Cheav T, Baroudi G, Berthet M, Denjoy I, Cauchemez B, Extramiana F, Chahine M, Guicheney P. Homozygous SCN5A mutation in long-QT syndrome with functional two-to-one atrioventricular block. Circ Res. 2001 Jul 20;89(2):E16-21. doi: 10.1161/hh1401.095087. PMID: 11463728.